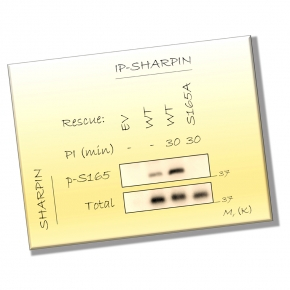
Phosphorylation de SHARPIN et NF-?B : la marque à suivre
Le complexe d’ubiquitination LUBAC orchestre l’activation du facteur de transcription NF-kB, une étape décisive de la réponse immunitaire innée et adaptative. Cette étude réalisée au Centre de Recherche en Cancérologie et Immunologie Nantes-Angers (CRCINA - INSERM/CNRS/Université de Nantes) et publiée dans la revue iScience, révèle que la phosphorylation de la sous-unité SHARPIN module l’activité de ce complexe et autorise l’activation optimale de NF-kB, un élément central dans l’immunité innée et adaptative. Ces résultats permettent d’envisager de nouvelles stratégies destinées à moduler l’action de ce complexe enzymatique.
L’ubiquitination est une modification post-traductionnelle impliquée dans la plupart des fonctions cellulaires chez les Eucaryotes. L’ubiquitination consiste en la liaison covalente d’ubiquitine, seule ou sous forme de chaînes, à un substrat. La topologie de ces chaînes fonctionne tel un véritable code et détermine la destinée des protéines ciblées. Le LUBAC (linear ubiquitin chain assembly complex), formé des enzymes HOIP et HOIL1 ainsi que de la protéine adaptatrice SHARPIN, catalyse la formation de chaînes d’ubiquitine atypiques dites « linéaires » et leur attachement spécifique à certains substrats. Le LUBAC gouverne notamment l’activation du facteur de transcription NF-kB en aval de la plupart des immunorécepteurs, assurant ainsi l’expression de gènes essentiels pour la mise en place de la réponse immune innée et adaptative. Toutefois, comment le LUBAC est régulé reste mal compris.